Nội Dung
Hướng dẫn giải Bài 5: Nguyên tố hóa học, sách giáo khoa Hóa học 8. Nội dung bài Giải bài 1 2 3 4 5 6 7 8 trang 20 sgk Hóa học 8 bao gồm đầy đủ đầy đủ lý thuyết, công thức, phương trình hóa học, chuyên đề hóa học, … có trong SGK để giúp các em học sinh học tốt môn hóa học lớp 8.
Lý thuyết
I. Nguyên tố hoá học là gì?
1. Định nghĩa
– Nguyên tố hoá học là tập hợp những nguyên tử cùng loại có cùng proton trong hạt nhân.
– Số p là số đặc trưng của nguyên tố hoá học.
2. Kí hiệu hoá học
– Kí hiệu hoá học biểu diễn ngắn gọn nguyên tố hoá học.
– Mỗi nguyên tố hoá học dược biểu diễn bằng 1 hay 2 chữ cái. Trong đó chữ cái đầu được viết ở dạng chữ in hoa gọi là kí hiệu hoá học.
– Cách viết kí hiệu hóa học:
+ Chữ thứ nhất viết in hoa. Ví dụ: Cacbon: C, hidro: H, oxi: O.
+ Chữ thứ hai nếu có viết thường nhỏ hơn. Ví dụ: Sắt: Fe, Natri: Na, Canxi: Ca.
II. Nguyên tử khối
– Nguyên tử khối có khối lượng rất nhỏ bé. Nếu tính bằng gam thì có số trị rất nhỏ.
– Khối lượng 1 nguyên tử C = 1,9926.\({10^{ – 23}}\)g.
Quy ước: \(\frac{1}{{12}}\) KLNT C làm đơn vị khối lượng nguyên tử gọi là đơn vị cacbon (viết tắt là đvC).
1đvC = \(\frac{1}{{12}}\) Khối lượng nguyên tử C
Ví dụ: C = 12 đvC; H = 1 đvC; O = 16 đvC; S = 32 đvC
– Khối lượng tính bằng đvC chỉ là khối lượng tương đối giữa các nguyên tử ⇒ Nguyên tử khối.
⇒ Định nghĩa: Nguyên tử khối là khối lượng của nguyên tử tính bằng đvC.
Ví dụ: Na = 23 , Al = 27 , Fe = 56 …
III. Có bao nhiêu nguyên tố hoá học?
– Có hơn 110 nguyên tố hoá học.
+ 92 nguyên tố tự nhiên.
+ Còn lại: nguyên tố nhân tạo. Năm 2016 có thêm 4 nguyên tố mới có tên gọi tạm thời là: ununtri, ununpenti, ununseptium và ununoctium. Một nhóm nghiên cứu Nga – Mỹ đã cùng phát hiện ra nguyên tố 115, 117 và 118, trong khi các nhà nghiên cứu Nhật Bản khám phá ra nguyên tố 113. Các nguyên tố này không tìm thấy trong tự nhiên mà được tổng hợp nhân tạo từ phòng thí nghiệm.
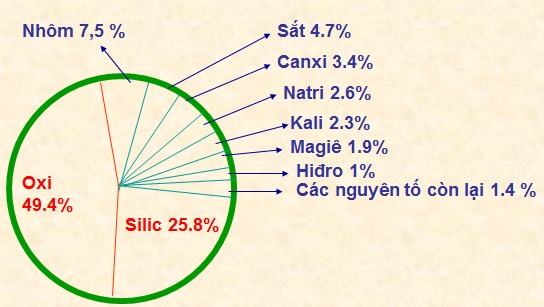
– Các nguyên tố tự nhiên có trong vỏ Trái Đất rất không đồng đều:
+ Oxi là nguyên tố phổ biến nhất: 49,4%.
+ 9 nguyên tố chiếm: 98,6%.
+ Nguyên tố còn lại chiếm: 1,4%.
Dưới đây là phần Hướng dẫn Giải bài 1 2 3 4 5 6 7 8 trang 20 sgk Hóa học 8. Các bạn hãy đọc kỹ đầu bài trước khi giải nhé!
Bài tập
Giaibaisgk.com giới thiệu với các bạn đầy đủ phương pháp trả lời các câu hỏi, giải các bài tập hóa học 8 kèm bài giải, câu trả lời chi tiết bài 1 2 3 4 5 6 7 8 trang 20 sgk Hóa học 8 cho các bạn tham khảo. Nội dung chi tiết bài giải, câu trả lời từng bài tập các bạn xem dưới đây:
1. Giải bài 1 trang 20 sgk Hóa học 8
Chép vào vở bài tập những câu sau đây với đầy đủ các từ hay cụm từ thích hợp.
a) Đáng lẽ nói những … loại này, những … loại kia, thì trong hóa học nói … hóa học này … hóa học kia.
b) Những nguyên tử có cùng … trong hạt nhân đều là … cùng loại, thuộc cùng một … hóa học.
Trả lời:
a) Đáng lẽ nói những nguyên tử loại này, những nguyên tử loại kia thì trong hóa học nói là nguyên tố hóa học này, nguyên tố hóa học kia.
b) Những nguyên tử có cùng số proton trong hạt nhân đều là nguyên tử cùng loại, thuộc cùng một nguyên tố hóa học.
2. Giải bài 2 trang 20 sgk Hóa học 8
a) Nguyên tố hóa học là gì?
b) Cách biểu diễn nguyên tố? Cho thí dụ.
Trả lời:
a) Nguyên tố hóa học là tập hợp những nguyên tử cùng loại, có cùng số proton trong hạt nhân.
b) Mỗi nguyên tố hóa học được biểu diễn bằng một hay hai chữ cái đầu tiên trong tên latinh nguyên tố đó, trong đó chữ cái đầu tiên được viết dưới dạng in hoa, gọi là kí hiệu hóa học.
Thí dụ: H, Ca, Al.
3. Giải bài 3 trang 20 sgk Hóa học 8
a) Các cách viết 2C, 5O, 3Ca lần lượt chỉ ý gì?
b) Hãy dùng chữ số và kí hiệu hóa học diễn đạt các ý sau: Ba nguyên tử nitơ, bảy nguyên tử canxi, bốn nguyên tử natri.
Trả lời:
a) Ý nghĩa của các cách viết:
2C ⇔ hai nguyên tử cacbon.
5O ⇔ năm nguyên tử oxi.
3Ca ⇔ ba nguyên tử canxi.
b) Diễn đạt:
ba nguyên tử nitơ ⇔ 3N.
bảy nguyên tử canxi ⇔ 7Ca.
bốn nguyên tử natri ⇔ 4Na.
4. Giải bài 4 trang 20 sgk Hóa học 8
Lấy bao nhiêu phần khối lượng của nguyên tử cacbon làm đơn vị cacbon? Nguyên tử khối là gì?
Trả lời:
Lấy \(\frac{1}{{12}}\) khối lượng của nguyên tử cacbon làm đơn vị cacbon.
Nguyên tử khối là khối lượng của một nguyên tử tính bằng đơn vị cacbon.
5. Giải bài 5 trang 20 sgk Hóa học 8
Hãy so sánh xem nguyên tử magie nặng hơn hay nhẹ hơn bao nhiêu lần so với :
a) Nguyên tử cacbon.
b) Nguyên tử lưu huỳnh.
c) Nguyên tử nhôm.
Trả lời:
– Giữa hai nguyên tử magie và cacbon, magie nặng hơn, bằng \(\frac{{24}}{{12}} = 2\) lần.
– Giữa nguyên tử magie và lưu huỳnh, magie nhẹ hơn nguyên tử lưu huỳnh, bằng \(\frac{{24}}{{32}} = \frac{3}{4}\) lần.
– Giữa nguyên tử magie và nguyên tử nhôm, magie nhẹ hơn nguyên tử nhôm, bằng \(\frac{{24}}{{27}} = \frac{8}{9}\) lần.
6. Giải bài 6 trang 20 sgk Hóa học 8
Nguyên tử X nặng gấp hai lần nguyên tử nitơ. Tính nguyên tử khối và cho biết X thuộc nguyên tố nào? Viết kí hiệu hóa học của nguyên tố đó.
Trả lời:
Nguyên tử khối của N = 14 đvC
⇒ Nguyên tử khối của X = 2 x 14 = 28 (đvC)
Vậy X là nguyên tố silic (Si).
7. Giải bài 7 trang 20 sgk Hóa học 8
a) Theo giá trị khối lượng tính bằng gam của nguyên tử cacbon cho trong bài học, hãy tính xem một đơn vị cacbon tương ứng với bao nhiêu gam?
b) Khối lượng tính bằng gam của nguyên tử nhôm là A, B, C hay D?
A. 5,324.10-23g.
B. 6,023.10-23g.
C. 4,482.10-23g.
D. 3,990.10-23g.
Trả lời:
a) Khối lượng của một nguyên tử cacbon bằng: 1,9926.10-23 (g) = 12 đvC.
⇒ 1 đvC = \(\frac{1,9926.10^{-23}}{12}\) ≈ 1,66.10-24 (g).
b) Khối lượng tính bằng gam của nguyên tử nhôm là:
mAl = 27 đvC = 27. 1,66.10-24 = 4,482.10-23 (g)
⇒ Chọn đáp án: C.
8. Giải bài 8 trang 20 sgk Hóa học 8
Nhận xét sau đây gồm hai ý: Nguyên tử đơteri thuộc cùng nguyên tố hóa học với nguyên tử hiđro vì chúng đều có 1 proton trong hạt nhân”. Cho sơ đồ thành phần cấu tạo của hai nguyên tử như hình vẽ bên:

Hãy chọn phương án đúng trong số các phương án sau:
A. Ý (1) đúng, ý (2) sai.
B. Ý (1) sai, ý (2) đúng.
C. Cả hai ý đều sai.
D. Cả hai ý đều đúng.
Trả lời:
⇒ Chọn đáp án D: (Cả hai ý đều đúng).
Câu trước:
Câu tiếp theo:
Xem thêm:
- Giải các bài tập Hóa học lớp 8 khác
- Để học tốt môn Toán lớp 8
- Để học tốt môn Vật lí lớp 8
- Để học tốt môn Sinh học lớp 8
- Để học tốt môn Ngữ văn lớp 8
- Để học tốt môn Lịch sử lớp 8
- Để học tốt môn Địa lí lớp 8
- Để học tốt môn Tiếng Anh lớp 8
- Để học tốt môn Tiếng Anh lớp 8 thí điểm
- Để học tốt môn Tin học lớp 8
- Để học tốt môn GDCD lớp 8
Trên đây là phần Hướng dẫn Giải bài 1 2 3 4 5 6 7 8 trang 20 sgk Hóa học 8 đầy đủ và ngắn gọn nhất. Chúc các bạn làm bài môn Hóa học lớp 8 thật tốt!
“Bài tập nào khó đã có giaibaisgk.com“
