Nội Dung
Hướng dẫn giải Bài 18: Mol, sách giáo khoa Hóa học 8. Nội dung bài Giải bài 1 2 3 4 trang 65 sgk Hóa học 8 bao gồm đầy đủ đầy đủ lý thuyết, công thức, phương trình hóa học, chuyên đề hóa học, … có trong SGK để giúp các em học sinh học tốt môn hóa học lớp 8.
Lý thuyết
I. Mol là gì?
Mol (n) là lượng chất chứa 6. 1023 nguyên tử hoặc phân tử chất đó.
Con số 6 .1023 được gọi là số Avogadro và được kí hiệu là N.
Ví dụ:
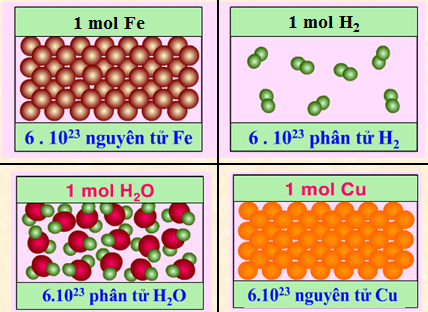
Lưu ý: Phân biệt ý nghĩa của 2 cách viết sau:
1 mol H ⇒ Chỉ 1 mol nguyên tử Hiđro
1 mol H2 ⇒ Chỉ 1 mol phân tử Hiđro
II. Khối lượng mol là gì?
– Khối lượng mol là khối lượng của N hạt phân tử hay nguyên tử chất đó.
– Khối lượng mol kí hiệu là M.
– Khối lượng mol của một chất có trị số bằng trị số của phân tử khối hoặc nguyên tử khối chất đó.
Ví dụ:
| Nguyên tử khối (hoặc phân tử khối) của một chất | Khối lượng mol nguyên tử (hoặc phân tử) của một chất |
| Nguyên tử khối của Fe là: 56 đvC | MFe = 56 (gam) |
| Phân tử khối của H2 là: 1×2 = 2 đvC | \({M_{{H_2}}} = 1 \times 2 = 2(gam)\) |
| Phân tử khối của H2O là: 1×2 + 16 = 18 đvC | \({M_{{H_2}O}} = 18(gam)\) |
+ Khối lượng mol nguyên tử Hidro: MH = 1 gam/mol
+ Khối lượng mol phân tử H2O : \({M_{{H_2}O}} = (1 \times 2 + 16) = 18(gam/mol)\)
– Lưu ý: Phân biệt ý nghĩa của 2 cách viết sau:
+ MN: Chỉ khối lượng mol nguyên tử Nitơ.
+ \({M_{{N_2}}}\): Chỉ khối lượng mol phân tử Nitơ.
III. Thể tích mol của chất khí là gì?
Thể tích mol chất khí (V) là thể tích chiếm bởi N phân tử chất khí đó.

Điều kiện tiêu chuẩn (đktc): 00C và 1atm, 1 mol khí chiếm 22,4 lít
Vậy: \({V_{{H_2}}} = {V_{{O_2}}} = {V_{C{O_2}}} = 22,4(lit)\)
Ở điều kiện bình thường là 200C và 1atm: 1 mol khí chiếm 24 lít.
Vậy: \({V_{{H_2}}} = {V_{{O_2}}} = {V_{C{O_2}}} = 24(lit)\)
Dưới đây là phần Hướng dẫn Giải bài 1 2 3 4 trang 65 sgk Hóa học 8. Các bạn hãy đọc kỹ đầu bài trước khi giải nhé!
Bài tập
Giaibaisgk.com giới thiệu với các bạn đầy đủ phương pháp trả lời các câu hỏi, giải các bài tập hóa học 8 kèm bài giải, câu trả lời chi tiết bài 1 2 3 4 trang 65 sgk Hóa học 8 cho các bạn tham khảo. Nội dung chi tiết bài giải, câu trả lời từng bài tập các bạn xem dưới đây:
1. Giải bài 1 trang 65 sgk Hóa học 8
Em hãy cho biết số nguyên tử hoặc phân tử có trong mỗi lượng chất sau:
a) 1,5 mol nguyên tử Al.
b) 0,5 mol nguyên tử H2.
c) 0,25 mol phân tử NaCl.
d) 0,05 mol phân tử H2O.
Bài giải:
a) \(1,5\) mol nguyên tử Al có chứa \(1,5\) N nguyên tử Al hay \(1,5{\rm{ }}.6{\rm{ }}.{\rm{ }}{10^{23}} = {\rm{ }}9.{\rm{ }}{10^{23}}\) nguyên tử Al.
b) \(0,5\) mol phân tử H2 có chứa \(0,5\) N phân tử H2 hay \(0,5{\rm{ }}.6{\rm{ }}.{\rm{ }}{10^{23}} = {\rm{ }}3{\rm{ }}.{\rm{ }}{10^{23}}\) phân tử H2.
c) \(0,25\) mol phân tử NaCl có chứa \(0,25\) N phân tử NaCl hay \(0,25{\rm{ }}.6{\rm{ }}.{\rm{ }}{10^{23}} = {\rm{ }}1,5{\rm{ }}.{\rm{ }}{10^{23}}\) phân tử NaCl.
d) \(0,05\) mol phân tử H2O có chứa \(0,05\) N phân tử H2O hay \(0,05{\rm{ }}.6{\rm{ }}.{\rm{ }}{10^{23}} = {\rm{ }}0,3{\rm{ }}.{10^{23}}\) phân tử H2O.
2. Giải bài 2 trang 65 sgk Hóa học 8
Em hãy tìm khối lượng của:
a) 1 mol nguyên tử Cl và 1 mol phân tử Cl2.
b) 1 mol nguyên tử Cu và 1 mol phân tử CuO.
c) 1 mol nguyên tử C, 1 mol phân tử CO, 1 mol phân tử CO2.
d) 1 mol phân tử NaCl và 1 mol phân tử C12H22O11 (đường).
Bài giải:
Ta có:
a) \({M_{Cl}} = 35,5\,g/mol;\)
\({M_{C{l_2}}} = 35,5.2 = 71\,g/mol\).
b) \({M_{Cu}} = 64\,g/mol;\)
\({M_{CuO}} = 64.1 + 16.1 = 80\,g/mol\).
c) \({M_C} = 12\,g/mol;\)
\({M_{CO}} = 12.1 + 16.1 = 28\,g/mol;\)
\({M_{C{O_2}}} = 12.1 + 16.2 = 44\,g/mol\).
d) \({M_{NaCl}} = 23.1 + 35,5.1 = 58,5\,g/mol;\)
\({M_{{C_{12}}{H_{22}}{O_{11}}}} = 12.12 + 1.22 + 16.11 \)\(= 342\,g/mol\).
3. Giải bài 3 trang 65 sgk Hóa học 8
Em hãy tìm thể tích (ở đktc) của:
a) 1 mol phân tử CO2 ; 2 mol phân tử H2 ; 1,5 mol phân tử O2 ;
b) 0,25 mol phân tử O2 và 1,25 mol phân tử N2.
Bài giải:
a) Thể tích ở điều kiện tiêu chuẩn:
1 mol phân tử CO2: \(V_{CO_{2}}\) = 1.22,4 = 22,4 lít
2 mol phân tử H2: \(V_{H_{2}}\) = 2.22,4 = 44,8 lít
1,5 mol phân tử O2: \(V_{O_{2}}\) = 1,5.22,4 = 33,6 lít
b) 0,25 mol phân tử O2: \(V_{O_{2}}\) = 0,25.22,4 = 5,6 lít
1,25 mol phân tử N2. : \(V_{N_{2}}\) = 1,25.22,4 = 28 lít
⇒ Thể tích hỗn hợp: Vhh = 5,6 + 28 = 33,6 lít.
4. Giải bài 4 trang 65 sgk Hóa học 8
Em hãy cho biết khối lượng của N phân tử những chất sau:
H2O ; HCl ; Fe2O3 ; C12H22O11.
Bài giải:
Khối lượng của N phân tử các chất chính là khối lượng mol phân tử của các chất đã cho.
– Khối lượng mol phân tử H2O:
\({M_{{H_2}O}} = 1.2 + 16.1 = 18g\)
– Khối lượng mol phân tử HCl:
\({M_{HCl}}\; = 1 + 35,5 = 36,5{\text{ }}g\)
– Khối lượng mol phân tử Fe2O3:
\({M_{F{e_2}{O_3}}} = 56.2 + 16.3 = 160\,g\)
– Khối lượng mol phân tử C12H22O11:
\({M_{{C_{12}}{H_{22}}{O_{11}}}} = 12.12 + 1.22 + 16.11 = 342\,g\)
Câu trước:
Câu tiếp theo:
Xem thêm:
- Giải các bài tập Hóa học lớp 8 khác
- Để học tốt môn Toán lớp 8
- Để học tốt môn Vật lí lớp 8
- Để học tốt môn Sinh học lớp 8
- Để học tốt môn Ngữ văn lớp 8
- Để học tốt môn Lịch sử lớp 8
- Để học tốt môn Địa lí lớp 8
- Để học tốt môn Tiếng Anh lớp 8
- Để học tốt môn Tiếng Anh lớp 8 thí điểm
- Để học tốt môn Tin học lớp 8
- Để học tốt môn GDCD lớp 8
Trên đây là phần Hướng dẫn Giải bài 1 2 3 4 trang 65 sgk Hóa học 8 đầy đủ và ngắn gọn nhất. Chúc các bạn làm bài môn Hóa học lớp 8 thật tốt!
“Bài tập nào khó đã có giaibaisgk.com“

